Matéria: tudo que ocupa lugar no espaço e possui massa. (madeira)
Corpo: porção definida da matéria. (tronco)
Objeto: corpo feito pelo homem com o intuito de se utilizá-lo para algum fim. (banco de madeira)
É possível perceber que a matéria pode existir em três estados físicos diferentes, o sólido, o líquido e o gasoso. É também possível verificar que alguns corpos podem mudar de estado físico, ou seja, deixar de ser sólido e passar para líquido e do líquido passar para o estado gasoso. Um exemplo disso é a água, que pode existir no estado sólido (como gelo), no estado líquido (como água), ou no estado gasoso (como vapor). Sendo assim, estas transformações recebem nomes, tais como:
- fusão para a passagem do sólido para o líquido;
- solidificação para a passagem do estado líquido para o sólido;
- vaporização para a passagem do estado líquido para o gasoso. No entanto, a vaporização pode ser subdividida em:
- ebulição, que é induzida, ou seja, quando se fornece energia a um líquido para ele se transformar no estado gasoso. Exemplo: ferver água em uma panela.
- evaporação, que é a passagem do estado líquido para o gasoso de forma espontânea, ou seja, quando você não induz esta transformação. Um exemplo é uma roupa secando no varal, ou uma poça d’água que evapora pela ação do Sol.
- calefação, que é a passagem do líquido para o gasoso de forma instantânea, ou seja, é uma passagem muito rápida. Um exemplo é quando jogamos gotas d’água em uma panela quente, o que ocorre naquele momento é a calefação.
- Condensação para a passagem do estado gasoso para o líquido. Exemplo é a formação de gotículas na parte de fora de um copo com água gelada. Neste fenômeno o que se observa é que o ar (que contém vapor d’água) próximo da superfície do copo se resfria e o vapor d’água torna-se água líquida na superfície externa do copo. (As gotículas)
- Sublimação para a passagem direta do estado sólido para o gasoso e do gasoso para o sólido. Um exemplo de sublimação é a passagem da naftalina (que é sólida) para o estado gasoso, diretamente sem que passe pelo estado líquido. A naftalina é utilizada para espantar baratas e traças de gavetas e armários. Ela possui um odor característico.
A partir disso, pode-se desenvolver um esquema para facilitar o seu entendimento.
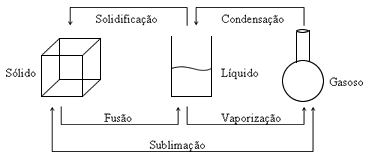 |
Estas transformações podem, também ser representadas graficamente. Nesta representação, aborda a temperatura de fusão e a temperatura de ebulição, pois se parte de um sólido e induz ele a passar pelos três estados físicos da matéria, para tal, basta fornecer energia a ele.
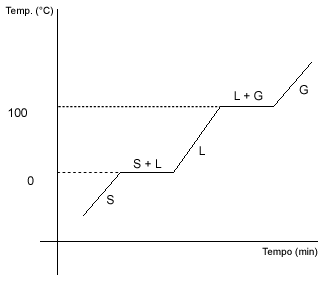 |
Tanto na temperatura de fusão e na temperatura de ebulição, a temperatura permanece constante, ou seja, existem duas fases presentes e a temperatura é constante. Isso para substâncias puras.
| Temperatura de fusão: temperatura constante na qual coexistem os estados sólido e líquido em equilíbrio. A temperatura será constante até que existam as duas fases. Temperatura de ebulição: temperatura constante na qual coexistem os estados líquido e gasoso em equilíbrio. A temperatura será constante até que existam as duas fases. |
Nos intervalos entre fusão e ebulição, a temperatura aumenta com o decorrer do tempo e o líquido vai aquecendo até que ele comece a ferver, aí teremos início a ebulição.
A partir deste gráfico também é possível verificar a temperatura de condensação e a temperatura de solidificação que são as mesmas que a temperatura de ebulição e temperatura de fusão, respectivamente.
Quando uma mistura sofre fusão e ebulição a uma temperatura constante, ou seja, a transformação inicia e termina a uma mesma temperatura, temos uma substância pura, ou substância.
| Quando uma amostra sofre fusão e/ou ebulição e a temperatura varia no momento da fusão ou da ebulição, temos uma mistura. Esta mistura pode ser azeotrópica quando a variação é na temperatura de fusão, ou a mistura pode ser eutética quando a variação de temperatura é na temperatura de ebulição. |
Misturas Azeotrópicas
São misturas que têm a temperatura de fusão variante, ou melhor, a fusão ocorre em uma faixa de temperatura como pode ser vista no diagrama abaixo.
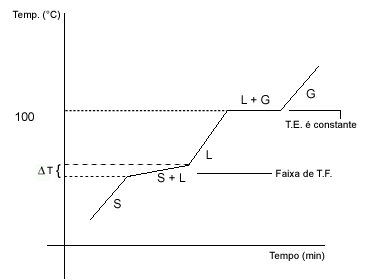 |
| Diagrama de fases para mistura azeotrópica |
Um exemplo de mistura azeotrópica é o álcool comercial, que ainda é vendido nos supermercados. Ele é uma mistura de 92,8% de álcool e 7,2% de água. (álcool Minalcool)
Misturas Eutéticas
São misturas que tem variação na temperatura de ebulição, ou melhor a ebulição ocorre em uma faixa de temperatura e não mais em uma temperatura constante. Isso pode ser visto no diagrama de fases, abaixo.
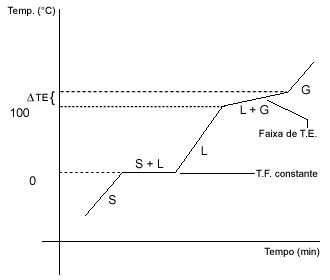 |
| Diagrama de fases para mistura eutética |
Um exemplo de mistura eutética é a mistura de gelo e sal de cozinha, que sofre fusão à temperatura constante, mas a ebulição ocorre em uma faixa de temperatura.


Nenhum comentário:
Postar um comentário
Comentem essa matéria, mas evitem usar links e escrever palavrões. Obrigado